
الخميس 12 مارس 2026 02:53 صباحاً صدر الصورة، Getty Images
يعمل الذكاء الاصطناعي على ابتكار أدوية جديدة لمواجهة مرض باركنسون، والبكتيريا الخارقة المقاومة للمضادات الحيوية، والعديد من الأمراض النادرة، وهو تقدّم لم يكن كثير من العلماء يتخيلون إمكانية تحقيقه.
على مدى نحو نصف قرن، كانت البشرية تخسر تدريجياً معركتها ضد البكتيريا. فقد أصبحت أقوى الأسلحة التي نملكها في هذه المعركة، وهي المضادات الحيوية، أقل فاعلية مع انتشار مقاومة الأدوية. ويُقدَّر أن نحو 1.1 مليون شخص يموتون سنوياً بسبب عدوى كان من السهل علاجها حتى وقت قريب. ومن المتوقع أن يرتفع عدد الوفيات إلى أكثر من ثمانية ملايين بحلول عام 2050 ما لم تُتخذ إجراءات عاجلة.
إن تطوير مضادات حيوية جديدة عملية بطيئة ومكلفة للغاية. فبين عامي 2017 و2022، تمت الموافقة على 12 مضاداً حيوياً جديداً فقط للاستخدام، وكان معظمها مشابهاً لأنواع أدوية موجودة بالفعل بدأت البكتيريا تطوّر مقاومة لها. وقد عانى هذا المجال من إهمال مزمن بسبب ضعف اهتمام شركات الأدوية ونقص التمويل.
لكن الباحثين يسعون الآن إلى سد هذه الفجوة - ويراهن بعضهم على الذكاء الاصطناعي للمساعدة في تحقيق ذلك.
ويقول جيمس كولينز، أستاذ الهندسة الطبية والعلوم في معهد ماساتشوستس للتكنولوجيا في كامبريدج بالولايات المتحدة: "يمكننا - خلال أيام أو حتى ساعات - فحص مكتبات ضخمة من المركبات الكيميائية" لتحديد تلك التي تُظهر نشاطاً مضاداً للبكتيريا.
وبمساعدة الذكاء الاصطناعي، تمكن كولينز وفريقه بالفعل من اكتشاف مركبين جديدين قد يشكلان سلاحين مهمين في مواجهة العدوى شديدة المقاومة للأدوية، مثل السيلان وجرثومة المكورات العنقودية الذهبية المقاومة للميثيسيلين.
يمثل ذلك مجرد مثال واحد على كيفية فتح الذكاء الاصطناعي لعصر جديد في اكتشاف الأدوية – مع وعود بإحراز تقدم في بعض أعقد المشكلات الطبية في عصرنا. ويقوم العلماء اليوم بتوجيه تقنيات الذكاء الاصطناعي نحو أمراض لا يُعرف لها علاج حتى الآن، مثل مرض باركنسون، وآلاف الأمراض النادرة، أملاً في تحقيق اختراقات جديدة.
درّب كولينز وفريقه نموذجاً من الذكاء الاصطناعي التوليدي للتعرّف إلى البُنى الكيميائية للمضادات الحيوية المعروفة. وقد أتاح ذلك للخوارزمية أن تتعلّم ما الذي يلزم لقتل البكتيريا. ثم استخدم الباحثون الذكاء الاصطناعي لفحص أكثر من 45 مليون بنية كيميائية مختلفة، بهدف تقييم قدرتها على استهداف بكتيريا النيسرية البنية، المسببة لمرض السيلان، وبكتيريا المكورات العنقودية الذهبية، وهي مصدر رئيسي للعدوى، بما في ذلك سلالات المكورات العنقودية الذهبية المقاومة للميثيسيلين.
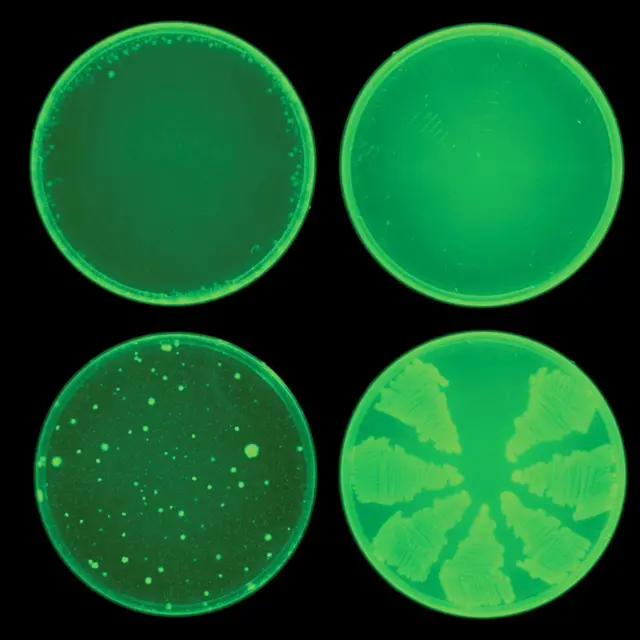
صدر الصورة، Collins Lab/ MIT
يتمتع كل نوع من هذين النوعين من البكتريا بدرجة عالية من مقاومة الأدوية - ففي حالة السيلان، باتت البكتيريا قادرة على مقاومة تأثير معظم الأدوية المستخدمة لعلاجه. ولم يتبقَّ اليوم سوى عدد متناقص من المضادات الحيوية المتاحة – وهي أدوية تُستخدم كحلّ أخير – لمواجهة كلٍ منهما.
وقد اعتمدت طريقة كولينز على استخدام الذكاء الاصطناعي لإنشاء مركّبات جديدة تماماً تستهدف هذه الجراثيم. ففي إحدى المقاربات، اختار جزيئاً كنقطة انطلاق، ثم استخدم مزيجاً من تقنيات الذكاء الاصطناعي التوليدي لتطويره تدريجياً، عبر "إضافة روابط وذرات وبُنى فرعية"، على حد قوله.
وفي كل مرحلة حاسمة، كان النموذج الذي درّبه فريقه من الذكاء الاصطناعي يقيّم المركّب الجديد عبر طرح أسئلة مثل:
"هل يبدو هذا كمضاد حيوي؟ وهل يقترب أكثر من أن يكون مضاداً حيوياً محتملاً؟"
أما المقاربة الأخرى فكانت تقوم على الاستغناء عن الجزيء الابتدائي تماماً، وترك الذكاء الاصطناعي يبتكر المركّبات من الصفر.
صمّم كولينز وزملاؤه بهذه الطريقة نحو 36 مليون مركّب كيميائي يُحتمل أن تكون فعّالة ضد هذه البكتيريا. واختار الفريق 24 مركّباً منها لتصنيعها في المختبر. وقد تبيّن أن سبعة مركّبات تمتلك نشاطاً مضاداً للميكروبات بدرجات متفاوتة، بينما أظهر مركّبان فعالية كبيرة في القضاء على سلالات من البكتيريا كانت مقاومة لأنواع أخرى من المضادات الحيوية.
والأهم من ذلك أن هذه المركّبات تبدو وكأنها تستهدف البكتيريا بطرق مختلفة عن المضادات الحيوية الموجودة حالياً، وهو ما يعزز الآمال في أن تشكّل فئة جديدة من الأدوية القادرة على تجاوز دفاعات البكتيريا المقاومة للعلاج. ويخضع المرشحان الدوائيان حالياً لمزيد من الاختبارات.
وقد استخدم كولينز وفريقه في مختبره الذكاء الاصطناعي سابقاً لاكتشاف مركّبات جديدة قوية من المضادات الحيوية قادرة على قتل مجموعة واسعة من البكتيريا المقاومة للعلاج، من بينها كلوستريديوم ديفيسيل، وهي بكتيريا تسبب عدوى معوية شائعة، والمتفطرة السلية المسببة لمرض السل.
لكن بالنسبة لبعض الأمراض، لا يملك الباحثون رفاهية الاستفادة من الأدوية الموجودة للمساعدة في اكتشاف علاجات جديدة. وبدلاً من ذلك، عليهم أن يبدأوا بما هو معروف عن المرض نفسه. وفي بعض الحالات، يكون حتى هذا القدر من المعرفة محدوداً للغاية.
تقدم في أبحاث باركنسون
تم التعرف إلى مرض باركنسون لأول مرة عام 1817، لكن بعد أكثر من قرنين من الزمن لا يزال لا يوجد علاج قادر على إبطاء تطور المرض. ويُقدَّر عدد المصابين بباركنسون في العالم بأكثر من 10 ملايين شخص، كما أن معدلات الإصابة به في تزايد في البلدان ذات السكان المتقدمين في السن.
وفي المملكة المتحدة، يُتوقع أن يُشخَّص نحو شخص واحد من كل 37 شخصاً بالمرض في مرحلة ما من حياته. أما في الولايات المتحدة، فيعيش حالياً ما يصل إلى مليون شخص مع هذا المرض.
تتخلل الجهود الطويلة لإيجاد علاج لمرض باركنسون سلسلة من الإخفاقات. وجزء من المشكلة يتمثل في أننا لا نزال حتى اليوم لا نعرف السبب الدقيق للمرض.
يقول ميشيل فيندروسكولو، أستاذ الفيزياء الحيوية والمشارك في إدارة مركز الأمراض المتعلقة بالبروتينات في جامعة كامبريدج في المملكة المتحدة: "هناك نقاشات لا تنتهي حول أصل هذا الاضطراب. فإذا حضرت مؤتمراً عن باركنسون، ستسمع عشرات الفرضيات المختلفة التي يجري التحقيق فيها بنشاط".
لكن هذا الغموض يجعل استهداف دواء يمكنه الوقاية من المرض أمراً بالغ الصعوبة.
ويقول فيندروسكولو إن عدداً هائلاً من التجارب السريرية أُجري لاختبار فرضيات مختلفة، إلا أنها لم تنجح حتى الآن. ويضيف: "الناس في حالة ارتباك حقيقي بشأن ما ينبغي أن يكون الهدف العلاجي. وحتى إذا عرفت الهدف، فإن استهدافه يكون في العادة أمراً شديد الصعوبة".
لكن في عام 2024 نشر فيندروسكولو وزملاؤه دراسة استخدموا فيها التعلّم الآلي - وهو أحد أشكال الذكاء الاصطناعي - للبحث عن مرشحين دوائيين محتملين قادرين على استهداف تكتلات البروتينات سيئة الطيّ في الدماغ لدى مرضى باركنسون.
وتُعرف هذه التكتلات البروتينية باسم أجسام ليوي، ويُعتقد أنها تلعب دوراً في المراحل الأولى من التنكس العصبي لدى مرضى باركنسون، وهو ما يؤدي لاحقاً إلى ظهور أعراض مثل الرعاش، وبطء الحركة، وتيبّس العضلات.
حالياً، يُعدّ ليفودوبا العلاج الأكثر فاعلية لمرض باركنسون، وهو دواء يساعد على تخفيف أعراض المرض، لكنه قد يسبب أيضاً آثاراً جانبية مثل الحركات اللاإرادية.
ويركز فيندروسكولو على إيقاف تطور المرض نفسه. وقد بدأ هو وفريقه بمجموعة من المركّبات التي كان قد تم تحديدها مسبقاً على أنها قد تكون فعّالة في استهداف أجسام ليوي. ثم أدخل هذه المركّبات في برنامج للتعلّم الآلي، قام بدوره باستنتاج مركّبات جديدة محتملة اعتماداً على بُناها الكيميائية، يمكن أن تكون بدورها فعّالة أيضاً.

صدر الصورة، Getty Images
لعلاج الأمراض التنكسية العصبية مثل باركنسون، يجب أن تكون الأدوية صغيرة بما يكفي لعبور الحاجز الدموي الدماغي. لكن حتى عندما يقيّد العلماء بحثهم بالجزيئات الصغيرة، فإن "خياراتهم تظل هائلة للغاية"، كما يقول فيندروسكولو. ويضيف: "عدد الجزيئات الصغيرة الممكنة أكبر بكثير من عدد الذرات في الكون".
تكمن قوة الذكاء الاصطناعي في قدرته على تضييق نطاق هذا البحث بسرعة كبيرة.
ويقول فيندروسكولو: "يمكننا تحليل هذه البيانات وإجراء توقعات دقيقة جداً حول كيفية ارتباط الجزيئات المرشحة بالهدف، وعلى نطاق كان من غير الممكن تخيله حتى قبل بضع سنوات".
فباستخدام الأساليب التقليدية، كان بإمكان العلماء فحص نحو مليون جزيء خلال ستة أشهر وبتكلفة تصل إلى عدة ملايين من الجنيهات الإسترلينية. أما الآن، فيمكن إنجاز العملية نفسها خلال بضعة أيام مع فحص مليارات الجزيئات، وبتكلفة لا تتجاوز بضعة آلاف من الجنيهات.
بعد ذلك، جرى اختبار المركّبات التي اقترحها الذكاء الاصطناعي في المختبر. ويقول فيندروسكولو: "قمنا بقياس أيّ من المرشحين يرتبط فعلياً [بأجسام ليوي]، ثم أدخلنا هذه المعلومات مجدداً إلى برنامج التعلّم الآلي، حتى يتمكن من التعلّم من أخطائه".
في النهاية، تمكن الفريق من تحديد خمسة مركّبات جديدة واعدة بسرعة وكفاءة أكبر من الطرق التقليدية. كما أن المركّبات التي حدّدها الذكاء الاصطناعي كانت أكثر ابتكاراً بكثير مما كان يمكن اكتشافه باستخدام الأساليب التقليدية لتطوير الأدوية، بحسب فيندروسكولو.
وتخضع هذه المركّبات حالياً لمزيد من الاختبارات لمعرفة ما إذا كان يمكن استخدامها يوماً ما كعلاج لمرضى باركنسون.
ويأمل فيندروسكولو أن يتمكن الذكاء الاصطناعي مستقبلاً من إيقاف مرض باركنسون قبل أن يبدأ. وهو يستخدم هذه التقنية الآن للبحث عن جزيئات صغيرة يمكنها الارتباط بالبروتينات الفردية التي تكوّن أجسام ليوي، وذلك بينما تكون هذه البروتينات لا تزال في حالتها الطبيعية.
ويقول: "إذا تمكّنّا من تثبيت البروتينات في هذه الحالة عبر الارتباط بها، فإننا نكون قد منعنا حدوث مرض باركنسون – وهذا أفضل من علاجه بعد ظهوره".
استخدامات جديدة لأدوية قديمة
لا يعني علاج الأمراض دائماً اكتشاف أدوية جديدة. فقد تمكّن ديفيد فاجنباوم، الأستاذ المشارك في الطب في جامعة بنسلفانيا في الولايات المتحدة، من إنقاذ حياته باستخدام دواء موجود أصلاً لم يكن الأطباء ليفكروا في وصفه له.
ففي سن الخامسة والعشرين، وأثناء دراسته في كلية الطب، شُخّص فاجنباوم بنوع نادر من اضطراب يُعرف باسم مرض كاسلمان، وهو مرض يسبب تفاعلاً في جهاز المناعة يؤدي إلى تعطل وظائف الكبد والكليتين ونخاع العظم.
لم يستجب لأي من العلاجات المتاحة، وأخبره الأطباء أنهم وصلوا إلى طريق مسدود في محاولة علاجه.
وبعد أسابيع من إجراء اختبارات على دمه بنفسه، والبحث المكثف في الأدبيات الطبية، والتعامل مع نفسه كأنه فأر تجارب بشري، توصّل في النهاية إلى علاج محتمل: دواء بسيط يُدعى سيروليموس.
ويُستخدم هذا الدواء عادةً لدى مرضى زراعة الكلى لمنع الجسم من رفض العضو الجديد. لكن، في خطوة حيّرت أطباءه، استخدم فاجنباوم هذا الدواء وتمكّن من إجبار مرض كاسلمان على التراجع.
ومنذ ذلك الحين، ظل المرض في حالة هدوء لأكثر من عقد من الزمن.

صدر الصورة، M Scott Brauer
فتحت تجربته عينيه على الإمكانات الكبيرة الكامنة في آلاف الأدوية التي خضعت بالفعل لاختبارات السلامة الصارمة اللازمة لطرحها في الأسواق.
ومن خلال إعادة توظيف هذه الأدوية لعلاج أمراض أخرى، يمكن للمرضى الحصول على علاجات لم تكن لتصبح متاحة لهم لولا ذلك.
وفي عام 2022 أسس فاجنباوم منظمة غير ربحية تُدعى Every Cure، تستخدم تقنيات التعلّم الآلي لمقارنة آلاف الأدوية مع آلاف الأمراض. ثم تُختبر الخيارات الأكثر احتمالا في المختبرات أو تُرسل إلى أطباء مستعدين لتجربتها.
لكن رغم أن فاجنباوم يُعدّ من أبرز العلماء الذين استخدموا الذكاء الاصطناعي بهذه الطريقة، فإن باحثين آخرين يحققون بالفعل اختراقات مهمة. ففي كلية الطب بجامعة هارفارد، تمكّن نموذج للذكاء الاصطناعي من تحديد ما يقرب من ثمانية آلاف دواء معتمد يمكن إعادة توظيفها لعلاج 17 ألف مرض مختلف.
ويثبت الذكاء الاصطناعي فائدة خاصة في العثور على علاجات للأمراض النادرة التي غالباً ما تتجاهلها شركات الأدوية بسبب ضعف الحافز المالي الناتج عن قلة عدد المرضى المحتملين.
كما يتيح إعادة استخدام الأدوية الموجودة فرصة إضافية. ففي السنوات الأخيرة، حدّد الذكاء الاصطناعي إمكانات لإعادة توظيف علاجات موجودة لأمراض مثل متلازمة بيت - هوبكنز، وهو اضطراب كروموسومي نادر، ومرض الساركويد، وهو مرض التهابي نادر، إضافة إلى ورم ويلمز، وهو نوع نادر من سرطان الكلى يصيب الأطفال الصغار.
ومؤخراً، استخدم باحثون في جامعة ماكغيل في مونتريال في مقاطعة كيبيك الكندية الذكاء الاصطناعي لإعادة توظيف أدوية لعلاج التليف الرئوي مجهول السبب، وهو مرض رئوي نادر ومتفاقم يتميز بتندّب وتثخّن أنسجة الرئة. وقد اعتمدت مقاربتهم على نمذجة تطور المرض باستخدام نموذج للذكاء الاصطناعي.
يقول أحد الباحثين المشاركين في الدراسة، جون دينغ، الأستاذ المساعد في قسم الطب في جامعة ماكغيل: "معظم الأمراض المعقّدة تنتج عن تغيّر غير طبيعي في حالة الخلايا. فإذا تمكّنا من فهم كيف انتقلت الخلية من حالة سليمة إلى حالة غير طبيعية، فقد نتمكن من عكس هذه العملية أو إبطائها".
ولتحقيق ذلك، قام الباحثون أولاً باستخراج خلايا رئوية من مشاركين أصحاء ومن مرضى في مراحل مختلفة من تطور المرض، مستخدمين تقنيات متقدمة لتسلسل الحمض النووي بدقة عالية بهدف توليد كمية كبيرة من البيانات. وقد أتاح لهم ذلك رؤية كيف تتغير الخلايا على مدار مسار المرض.
بعد ذلك، طوروا نموذجاً توليدياً للذكاء الاصطناعي لمحاكاة هذه العملية، بحيث يقوم برسم خريطة لتحولات حالات الخلايا المختلفة وتغير أعدادها مع تقدم المرض. وخلال هذه العملية، كان النموذج يحدد أيضاً المؤشرات الحيوية التي يمكن استخدامها لتشخيص المرض، إضافة إلى أهداف علاجية محتملة.
يقول دينغ: "نحن نسميه النظام الافتراضي للمرض".
تقليدياً، كانت الأدوية تُختبر على الحيوانات أو على خلايا بشرية معزولة. لكن الباحثين أرادوا تطبيق الفكرة نفسها باستخدام الذكاء الاصطناعي - أي محاكاة تأثيرات مرض التليّف الرئوي مجهول السبب على خلايا افتراضية.
ويضيف دينغ: "يمكن للباحثين بعد ذلك اختبار تأثيرات استخدام أدوية مختلفة داخل هذا النموذج، من دون تكاليف كبيرة".
في دراسة جامعة ماكغيل، اقترح الذكاء الاصطناعي ثمانية خيارات علاجية محتملة لمرض التليّف الرئوي مجهول السبب. ومن بين أكثرها وعداً دواء يُستخدم عادةً لعلاج ارتفاع ضغط الدم، ما يوفّر خياراً منخفض التكلفة ثبتت سلامته بالفعل.
ويقول دينغ إن نظام الذكاء الاصطناعي الذي طوّره مع زملائه يمكن استخدامه أيضاً لدراسة أمراض أخرى، بما في ذلك السرطانات وأمراض الرئة المختلفة. ويواصل فريقه حالياً العمل على تحسين النموذج وتوسيعه ليشمل مجموعة أوسع من الحالات المرضية.
شهد التليّف الرئوي مجهول السبب اختراقاً حديثاً آخر بفضل الذكاء الاصطناعي. فقد طورت شركة إنسيليكو ميديسن المتخصصة في اكتشاف الأدوية باستخدام الذكاء الاصطناعي مركّباً دوائياً يُعرف باسم رينتوسيرتيب. وفي التجارب السريرية من المرحلة الثانية أظهر هذا الدواء نتائج واعدة في مواجهة المرض.واستخدمت الشركة الذكاء الاصطناعي لتحديد نقطة ضعف محتملة في المرض ثم لتصميم دواء قادر على استهدافها. وتأمل أنه في حال نجاح التجارب، قد يصبح الدواء متاحاً بحلول نهاية هذا العقد.
وليست إنسيليكو ميديسن وحدها في هذا المجال. فهناك شركات أخرى مثل تيراي وإيزومورفيك لابس وريكيرشن فارماسيوتيكلز وشرودنغر تعمل أيضاً على تحقيق تقدّم طبي باستخدام الذكاء الاصطناعي.
ويقول دينغ: "أعتقد أنه خلال السنوات الخمس إلى العشر المقبلة، قد يكون معظم تطوير الأدوية الجديدة موجهاً بالذكاء الاصطناعي، أو حتى قائماً عليه بالكامل".
ثورة محدودة
لكن رغم التقدم الذي يقوده الذكاء الاصطناعي، لا تزال هناك قيود. فالكثير من قواعد البيانات المتعلقة بالأدوية تحتفظ بها شركات التكنولوجيا الحيوية وشركات الأدوية، ما يعني أنها غير متاحة للعامة.
ويقول كولينز: "نحن بحاجة إلى بيانات حول خصائص الأدوية مثل الامتصاص والتوزيع والإخراج والسمّية. لكننا لا نملك هذه البيانات".
وفي الوقت الراهن، يكون الذكاء الاصطناعي أكثر فائدة في المراحل الأولى من عملية تطوير الأدوية، مثل تحديد الهدف العلاجي والبحث عن الجزيئات القادرة على الارتباط به. وهذه ليست سوى خطوتين من عملية طويلة ومعقدة لتطوير الأدوية الجديدة، ما يعني أن الأمر قد يستغرق وقتاً قبل أن تصل هذه العلاجات المحتملة إلى المرضى - إن وصلت أصلاً.
ويقول فيندروسكولو: "الذكاء الاصطناعي يُحدث ثورة في اكتشاف الأدوية… لكن بطرق محددة جداً".
تم ادراج الخبر والعهده على المصدر، الرجاء الكتابة الينا لاي توضبح - برجاء اخبارنا بريديا عن خروقات لحقوق النشر للغير








